Pfizer đã yêu cầu chính phủ Mỹ ngày 7/10 cho phép sử dụng vaccine Covid-19 cho trẻ em 5-11 tuổi, AP đưa tin. Nếu các cơ quan quản lý đồng ý, việc tiêm chủng có thể bắt đầu trong vòng vài tuần tới.
Pfizer thông báo trên Twitter rằng họ đã chính thức nộp đơn lên Cục Quản lý Thực phẩm và Dược phẩm (FDA).
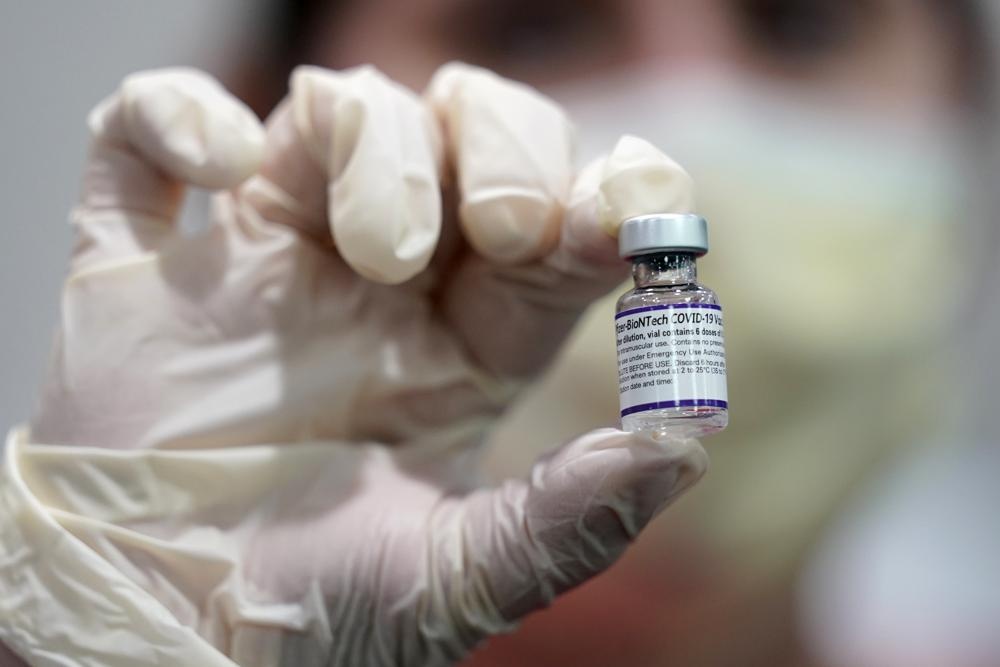 |
| Pfizer xin cấp phép sử dụng vaccine cho trẻ em từ 5-11 tuổi. Ảnh: AP. |
Giờ đây, FDA sẽ phải quyết định xem liệu có đủ bằng chứng cho thấy việc tiêm vaccine này an toàn và có hiệu quả với trẻ nhỏ như ở thanh thiếu niên và người lớn hay không. Một hội đồng chuyên gia độc lập sẽ có cuộc thảo luận mở về vấn đề này vào ngày 26/10.
Thông báo mới được đưa ra trong bối cảnh nhiều bậc cha mẹ và bác sĩ nhi khoa đang kêu gọi bảo vệ trẻ em dưới 12 tuổi sau khi các trường học được mở cửa trở lại, bất chấp làn sóng Covid-19 do biến chủng Delta gây ra.
Trước đó, ngày 20/9, Pfizer thông báo kết quả thử nghiệm lâm sàng giai đoạn 2-3 cho thấy vaccine phòng Covid-19 của hãng này an toàn và hiệu quả cho trẻ em từ 5-11 tuổi khi dùng liều lượng bằng 1/3 liều được sử dụng ở thanh thiếu niên và người trưởng thành.
Sau khi tiêm mũi thứ hai, trẻ từ 5-11 tuổi đã phát triển mức độ kháng thể tương đương nhóm lớn tuổi hơn.
Pfizer đã thực hiện nghiên cứu này ở hơn 2.268 tình nguyện viên từ 5-11 tuổi và cho biết không có tác dụng phụ nghiêm trọng.
Tuy nhiên, theo AP, nghiên cứu này chưa đủ quy mô để phát hiện những tác dụng phụ cực kỳ hiếm gặp, chẳng hạn viêm tim đôi khi xảy ra sau khi tiêm mũi vaccine thứ hai, chủ yếu ở nam giới trẻ tuổi.
Nếu FDA cho phép sử dụng khẩn cấp vaccine Pfizer cho trẻ em, vẫn sẽ có một "rào cản" khác trước khi kế hoạch tiêm chủng ở nhóm tuổi này được triển khai.
Các cố vấn của Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh (CDC) Mỹ sẽ phải xem xét để quyết định có nên khuyến nghị tiêm vaccine cho trẻ em hay không. CDC sẽ đưa ra quyết định cuối cùng.